外因系PTについて PT Information
PT検査は 凝固反応系の外因系を測定します。
これは組織因子を出発点として凝固が起こる経路で、非常に強力な凝固力を持つ系です。
その反応系の機序を概説すると、
① ケガや注射針を刺したとき、血管組織・細胞に一部が壊れ、細胞内部にあった組織片が表面露出し、血液と接触するようになります。この組織片のことを組織因子TF(第Ⅲ因子またはF.Ⅲ)と言います。
② F.Ⅲは、血液中に混在している第Ⅶ因子(F.Ⅶ)を活性化します。血液中のF.Ⅶは通常は何もしないただの蛋白質なのですが、F.Ⅲによって鞘から出され、むき出しのナイフとなります。これをF.Ⅶと区別する意味でF.Ⅶaと書きます。
③ F.Ⅶaは、血液中に混在している第Ⅹ因子(F.Ⅹ)を活性化します。F.Ⅹはこれもまた、血液中では通常は何もしないただの蛋白質なのですが、F.Ⅶaによって鞘から出され、むき出しのナイフ(F.Ⅹa)となります。
④ F.Ⅹaはリン脂質上で血液中の第Ⅴ因子と合体して、稼動し始め、プロトロンビン(F.Ⅱ)をトロンビン(F.Ⅱa)にします。
⑤ トロンビンは強力な酵素で、フィブリノーゲン(F.Ⅰ)をフィブリン(Fibrin)に変えて行きます。
⑥ フィブリンは凝固塊を形成し、止血します。
PT試薬はウサギ脳などから組織因子(=テッシュファクター:TF)を抽出したものです。これと
血漿成分とを混合すると、上記の反応が起こります。
血漿中に含まれる種々の凝固因子が適正量含まれ、適正な反応力を持つ場合には適正な時間で最
終的にフィブリン繊維が形成されます。が、凝固因子が不足していたり、あるいは活性が十分でな
い場合には凝固時間は延長します。凝固時間が延長する度合いは血漿が持っていた凝固活性の量と
して算出されます。
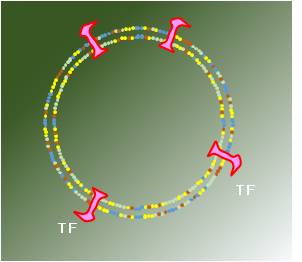
右図:PT試薬の構造(模式図)
りん脂質で構成されるマイクロパーティクルの表面に組織トロンボプラスチン蛋白質が露出
している。これをトリガーとして凝固反応が開始する。
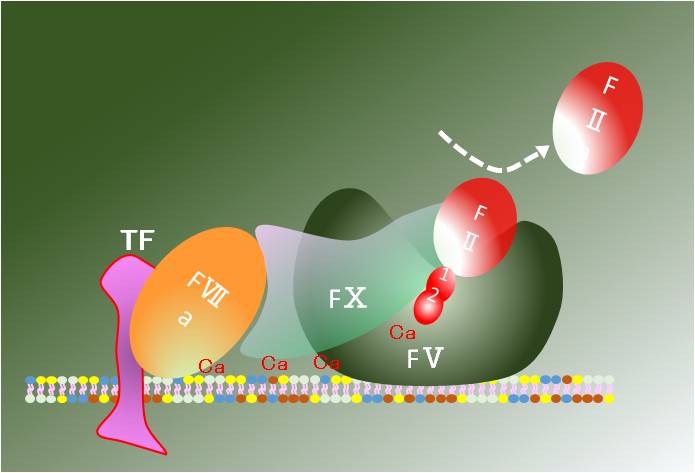
下図:外因系凝固因子複合体(模式図)
りん脂質表面に突出したTFに第Ⅶ因子が結合します。
りん脂質表面の陰性荷電の強い領域に第Ⅴ因子が結合し、その近傍にカルシウムを介して
第Ⅹ因子が結合します。
第Ⅶ・第Ⅴ・第Ⅹ因子の複合体が形成されると、第Ⅱ因子を活性化する機能が発現し、
トロンビンを造ります。トロンビンはフィブリノーゲンをフィブリンに変化させます。
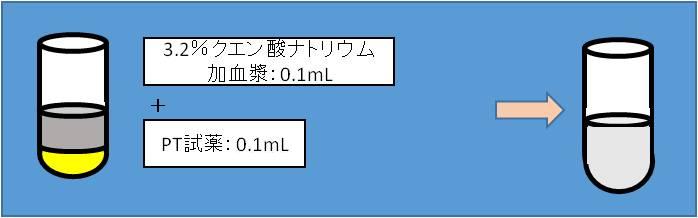
2. プロトロンビン時間(PT)の検出
PT時間は血漿と試薬が混合された後の白濁化する状況や粘度の違いによって検出されます。
用手法で測定されていた時期はヒトが試験管を振り、白濁の状況と粘度=固化の状況を目で確かめて
ストップウォッチで凝固時間を測定していました。これを機械的に自動化する段階になると、白濁の
状況は光学的変化として計算されるようになり、粘度変化はフィブリン繊維の検出する方法と粘張度
検出法に工夫されました。後者の検出器としてはKC-4が有名ですが、前者の光学的検出方法では散乱
光の変化量から凝固時間を算出する方法や、光学的変化を微分するなどの解析で凝固時間を算出する
方法、あるいはそれらの組み合わせを使う方法など多様な方法があります。
ここでは、光学的(散乱光)変化量から凝固時間を算出する方法を例にとって凝固時間の解析をして
みます。
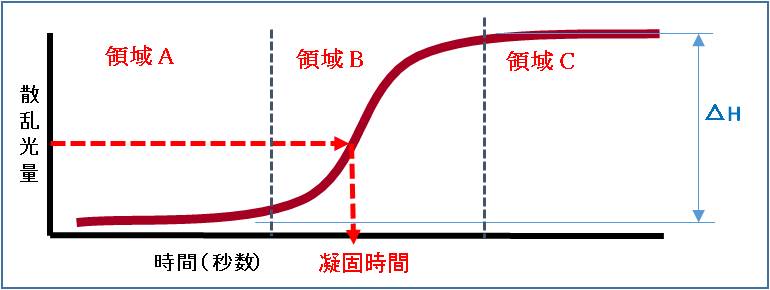
凝固反応はPT試薬を混合した直後では光学的変化=白濁は生じません。この間は組織トロンボプラ
スチンから初期フィブリンの形成までの反応が起こっていると考えられます。この領域をA領域と
します。
次に形成されたフィブリンが成長すると光学的変化となり、散乱光が増大してきます。フィブリン
分子は約90nmの大きさなので660nmの光を散乱する分子としては7分子以上のフィブリン分子が結合
した状態で初めて検出されるものと考えられます。フィブリン分子の重合が進むと繊維化し、散乱
光はさらに増大します。重合するフィブリンそのものが残り少なくなってくると散乱光の変化は少
なくなり、やがて光量の変化はなくなります。この領域をB領域とします。
凝固が終息すると散乱光の変化はなくなります。この領域をC領域とします。
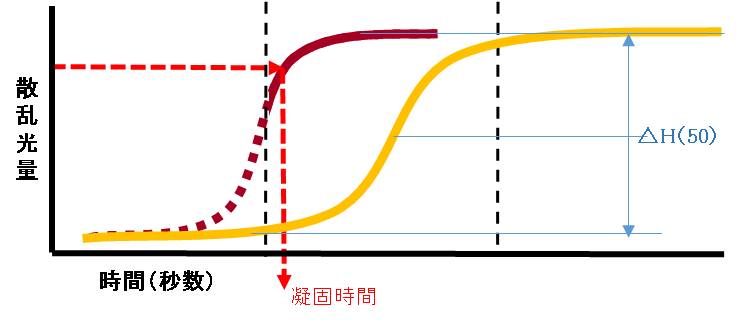
凝固時間は、例えばある機械では光量変化前のレベルを0%とし、光量変化が終息したレベルを100
%とし、その中間である50%(△H=50)を凝固時間とします。
他に、光学的変化を微分解析し、変化量0の変曲点を凝固時間とする方法、さらにはこれに各種計
算条件を設定する方法などがあります。(資料参照)
通常、一般的なPT試薬では試薬の混合・測定部への移動に約2秒を要し、撹拌による“ゆらぎ”
を安定させるためには3秒以上の時間が必要です。よって最低でも領域Aは5秒間以上の時間が確保
されていなくてはならないことになります。ヒト血漿の測定で凝固時間が10秒の場合、凝固曲線の
立ち上がりに4秒間を要するとすると、領域Aと領域Bの境目は6秒と言うことになり、5秒間は確
保されていると言えます。 測定結果として凝固時間が8秒以下の場合、領域Aは十分に確保されて
いないことに留意しておく必要があります。
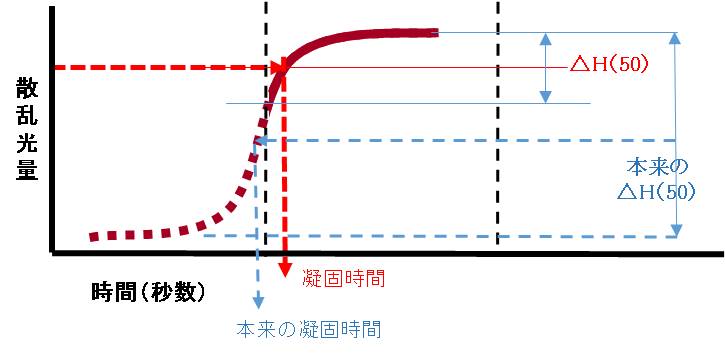
しかしながら、イヌなどの高活性な血漿では凝固時間が短いために、試薬と混合後すぐに散乱光が
増加する現象が現れます。すると、最低ラインの5秒間が確保されていませんので、凝固曲線の解
析は0レベルからではなく凝固曲線の途中から解析をせざるを得なくなります。その結果、凝固時
間は本来の結果より遅れた状態の値を算出することになります。
また、凝固時間は試薬特性により、短く表示されたり、逆に延長したりします。そのためイヌなど
の高凝固活性の血漿サンプルでは試薬特性の影響をより強く受ける傾向にあります。
領域Aが5秒間以上必要なことは物理的です。また試薬特性の差がないことも重要な要素です。
従ってPT試薬に求められる要素として、凝固時間は延長傾向を示すPT試薬であること、またロット
間ばらつきのを調整する技術が必要です。弊社(株式会社レイデックス)ではこの両方の問題を技
術的に解決した“ラビPT-N”、“ラビPT-L”をご提案しております。

3.活性% と INR
臨床検査測定は検体・試薬・機器(手技)の3要素から成ります。これら3つの要素が正確に且つ
継続的に運営されることが、良い治療方法へのフィードバックとなります。また、一か所の病院(検査室)
で測定結果が安定的に得られるだけでなく、検査する箇所全てで統一的且つ安定的なデータが得られるこ
とが望まれます。
しかしながらPT検査においては出発点においてPT試薬が各病院検査室で作られていた歴史があります。
その結果、臨床検査測定は検体・試薬・機器(手技)の3要素から成ると述べましたが、“試薬”は出発
時点から多様に富んでいたと言うことになります。また測定機器においても、当初は手振りで検出してい
ましたし、機器が提供されるようになっても各種の測定原理の異なる機器が用いられ、そのことに拠って
もデータは多様なものとなりました。採血についても同様で、PT測定では安定的且つ統一的な測定結果を
提供することが非常に難しい状況にありました。
それらを統一的に解析する努力も一方で試みられてきました。PT試薬や測定機器(手技)の多様性
を凌駕する形でPTの表現方法を工夫する方法です。
① 秒数
② 正常/異常
③ 異常/正常
④ 活性%の表示
⑤ INR表示
PT結果を報告する方法として、最初に利用された表現方法は ① 秒数で、これは現在でも使用して
いる施設があります。測定結果は概念的(感覚的)に異常の程度を推定することができます。また、継
続して観察すれば病態の経過を知ることができます。しかし、測定結果は試薬ロットによって変動し、
精密に比較するには問題があります。
②および、③ は秒数として概念的に把握するのではなく、より客観的な値として診るために工夫され
ました。この方法では、正常/正常 = 1.0 に対して、比としての値が高く表示されるか(または低く
表示されるか)によって、正常と比較した異常の程度を知ることができます。この場合、試薬ロット間
差の影響を受けにくくなり、秒数に比べればより客観的な値となります。けれども、同一の検査室の場
合には比較できますが、他施設との比較、あるいは種類の異なる試薬を使用する場合では、比較できな
くなります。
活性%を使用する方法は、今日、本邦では最も広く使用されています。使う試薬それぞれに検量線を
作成するので、秒数や比が異なっても、正常は100%と算出され、異常はその程度に応じて低値に表示
されます。この結果、活性%表示は多様な試薬間の比較ができ、標準化の手段として優れた方法である
と思われます。ただ、検量線が湾曲すると言う欠点もあります。
INR表示は、WHOのテクニカルレポート(1983、Geneva勧告(Recommended)において、。ワー
ファリン治療、あるいはそのモニタリングにおいて、活性%表示では湾曲する部分を直線的に表示する
方法として採用されています。国際標準PT試薬として、BCT/099が1978年に、1983年にはBCT/
253がヒト脳由来のトロンボプラスチン試薬としてが設定され、さらに1983年には、二次標準品として、
ヒト、ウシ、ウサギ脳由来のトロンボプラスチン製剤が設定されました。これらは、一次標準品と直接
比較検討されたISI値が付けられており、 ECの一部門であるBCRが認定標準材料としてその配布を
おこなうことにより、世界的に比較検討できるシステムが完成しました。
トロンボプラスチンにおいてWHOのIRPを使用する場合の方法をしています世界的標準化の検討
において考案された方法です。
INRは、検体の秒数=(A)を正常な検体の秒数=(B)で割り、それに試薬感度=ISI値を乗ずる方法です。
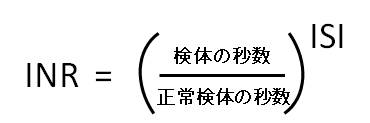
検体の秒数とは、測定したい対象のPT測定結果であり、正常検体の秒数とは20名以上の健康な男女の
測定結果(またはその平均値)です。ISIはPT試薬毎に設定された値であり、これは国際標準品に照らし
合わせて設定したものが各メーカーから参考値として表示されています。
今日、全自動化された機械ではそのほとんどで自動的にINR値が表示されるようになっています。